- 電子顕微鏡で観察すると、脂質二重層は“鉄道の線路のよう”に見える。重層のどのような構造がこうした像の原因か、説明せよ
- 生体膜は多種類の脂質分子を含む。生体膜に存在する3種類の主要な脂質分子は何か。これらはどこが似ていて、どこが違うか
- リン脂質に共有結合して細胞膜の細胞質側や反細胞質側に結合するタンパク質が存在する。そうしたタンパク質の係留に使われる3種類の脂質はどのようなものか。細胞外部に面した細胞表面タンパク質やグリコシル化されたプロテオグリカンを係留するのに使われているのはどれか
- 脂質二重層は,二次元の流動層と考えられる。これはどんな意味か.二重層内での脂質分子やタンパク質の動きを駆動するのは何か。こうした動きはどうやって測るのか。膜の流動性に影響を与える因子は何か
- 小胞体と細胞質の間でのリン脂質の生合成では、細胞によって解決されなければならない問題がいくつかある。以下のそれぞれはどのように対処されているか説明せよ。a. リン脂質の生合成の基質はすべて水溶性である。しかし、最終産物は水に不溶性である。b. すべての新しく生合成されたリン脂質を取込む箇所は、小胞体膜の細胞質側リーフレットである。しかし、リン脂質は膜の両側に組込まれなくてはならない。c. 細胞の多くの膜系(たとえば細胞膜)は、自身のリン脂質を合成することはできない。しかし、これらの膜は、細胞が成長したり分裂したりするとき、拡張されなければならない。
- 脂肪酸が細胞内で移動するためには脂質シャペロンが必要である。なぜそうしたシャペロンが必要なのか。脂肪酸の細胞内輸送にかかわっているタンパク質群は何とよばれているか。脂肪酸の細胞内輸送にかかわるこれらのタンパク質の重要な特徴は何か。
- グリセロリン脂質に共通する脂肪酸鎖は何か。また、なぜこれら脂肪酸鎖の炭素数は 2の倍数になっているのか。
- コレステロール生合成において、重要な調節を受ける酵素は何か。この酵素はフィードバック阻害を受ける。フィードバック阻害とは何か。この酵素は細胞内のコレステロール量をどのように感知するのか。
- コレステロールは哺乳類の細胞膜内において最も普遍的な脂質分子なので,その機能のひとつは構造の維持であることは明白である。しかし、コレステロールはほかにも機能をもっている。コレステロールは多機能的な膜脂質であるという結論に導くコレステロールとその代謝の特徴は何か。
- リン脂質とコレステロールは、細胞内の合成部位からさまざまな膜系へと輸送されなければならない。この方法のひとつは小胞輸送であり、多くのタンパク質を分泌する経路もこれによって行われる。しかし、ほとんどのリン脂質およびコレステロールの膜間輸送は、ゴルジ体を介した小胞輸送によるものではない。この記述の根拠は何か。また、リン脂質とコレステロール輸送のおもだった機構はどんなものか。
- 次の文章を説明せよ。すべての生体膜の構造は、リン脂質の化学的な性質に依存している。一方、特定の生体膜の機能は、この膜に結合した特定のタンパク質に依存している。
- 膜に結合しているタンパク質を三つに分類したとき、それぞれをどんな名称でよぶか、それぞれの分類に属するタンパク質が生体膜と結合する機構を解説せよ。
- 生体膜の両面は主として脂質やタンパク質といった同じような成分でできているが、両者の組成は同一ではない。何が両面の非対称性を生み出すか。
電子顕微鏡で観察すると、脂質二重層は“鉄道の線路のよう”に見える。重層のどのような構造がこうした像の原因か、説明せよ
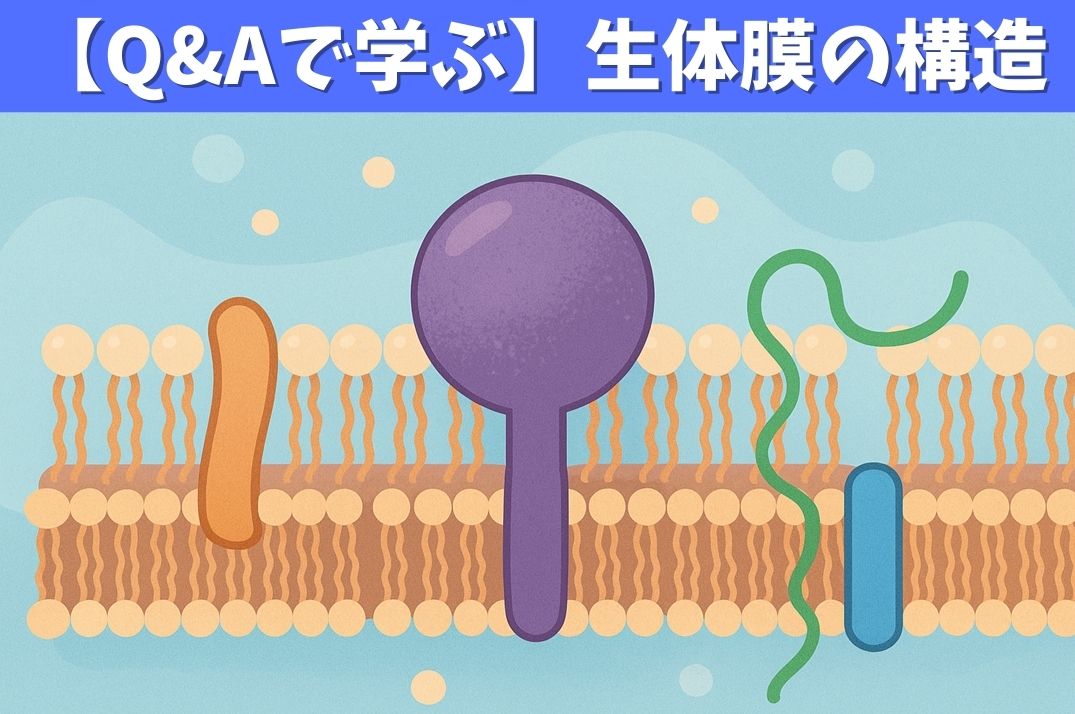
電子顕微鏡で脂質二重層(細胞膜)を観察すると、“鉄道の線路のよう”な像(2本の暗い線が並行し、その間にやや明るい部分がある)が現れます。この像が生じる理由は、脂質二重層の構造的特徴にあります。
構造とコントラストの関係
- 脂質二重層は、親水性のリン脂質「頭部」が外側(細胞外・細胞質側)に、疎水性の「脂肪酸鎖(尾部)」が内側に互いに向き合って配列しています。
- 固定および電子染色処理の過程で、親水性頭部はオスミウムなどの重金属染料をよく保持し、電子顕微鏡像上で「電子密度が高い=暗い線」として現れるのに対し、
- 中央の疎水性尾部(脂肪酸鎖の層)は染まりにくく「電子密度が低い=明るい帯状」として写ります。
「鉄道の線路のよう」なイメージの正体
- このため電子顕微鏡写真では、膜の断面が**「暗線(親水性頭部/外層)‐明線(疎水性尾部/内層)‐暗線(親水性頭部/内側)」**という三層構造で描出されます。
- この「2本の暗い線(親水性頭部)」と「その間の明るい帯(脂肪酸尾部)」が、まさに“鉄道の線路”のように見える原因です。
まとめ
脂質二重層が電子顕微鏡で鉄道の線路のように見えるのは、親水性リン脂質頭部が電子染色で強調されて暗線となり、疎水性脂肪酸鎖部分が比較的明るく写ることで、この特徴的な三層構造像が生じるためです。
生体膜は多種類の脂質分子を含む。生体膜に存在する3種類の主要な脂質分子は何か。これらはどこが似ていて、どこが違うか
1. リン脂質(Phospholipid)
- 代表:ホスファチジルコリン(PC)、ホスファチジルエタノールアミン(PE)、スフィンゴミエリン(SM)など
- 特徴:親水性の頭部(リン酸基+アルコール)と2本の疎水性脂肪酸鎖からなる“両親媒性分子”
- 主な役割:脂質二重層の最大構成成分。分子の両親媒性によって安定した二重層形成と細胞膜の選択的バリア機能を担う
2. 糖脂質(Glycolipid)
- 代表:ガングリオシド、セレブロシド、ガラクト脂質など
- 特徴:親水性頭部が糖(単糖やオリゴ糖)、疎水性部分はセラミド(スフィンゴシン+脂肪酸)やグリセロール由来
- 主な役割:細胞膜の外側に局在し、細胞認識やシグナル伝達、抗原性の決定などを担う
3. コレステロール(Cholesterol)(またはその他のステロール)
- 特徴:極性水酸基と疎水性の四環炭素骨格・短い側鎖からなる
- 主な役割:脂質二重層に挿入され、膜の流動性・剛性や透過性の調節を行う。両親媒性ではあるが、頭部は短い。
「似ている点」と「異なる点」
〈似ている点〉
- いずれも両親媒性分子(親水性の頭部+疎水性の脂肪鎖やステロール骨格)で構成され、脂質二重層の自発形成を支える。
- 膜の流動性や安定性に寄与し、生理機能を調節。
- 生体膜上で、タンパク質の局在や膜ドメイン形成などと密接に関連。
〈異なる点〉
| 脂質クラス | 主な構造の違い | 主な機能・分布 |
|---|---|---|
| リン脂質 | 頭部=リン酸基とアルコール | 二重層の骨格成分、内外層に分布 |
| 糖脂質 | 頭部=糖鎖(単糖・多糖) | 外層に多く、細胞認識・結合・情報伝達など |
| コレステロール | ステロイド環+短い極性基 | 二重層全体に存在、膜流動性と剛性の調節など |
- 骨格の違い:リン脂質は「グリセロール骨格」、糖脂質は「スフィンゴシンやグリセロール骨格」、コレステロールは「ステロール骨格」。
- 機能の違い:リン脂質は基礎的な骨格、糖脂質は認識や情報伝達、コレステロールは膜物性調節に特化。
まとめ:生体膜の3大脂質(リン脂質、糖脂質、コレステロール)はいずれも両親媒性ながら、構造や主機能・膜内での分布・役割が異なります。これにより細胞膜の多様性と機能性が支えられています。
リン脂質に共有結合して細胞膜の細胞質側や反細胞質側に結合するタンパク質が存在する。そうしたタンパク質の係留に使われる3種類の脂質はどのようなものか。細胞外部に面した細胞表面タンパク質やグリコシル化されたプロテオグリカンを係留するのに使われているのはどれか
細胞膜にタンパク質を脂質修飾(共有結合)によって係留する場合、主に使われる脂質は以下の3種類です。
1. ミリスチン酸(Myristic acid)
- 修飾名:ミリストイル化
- 特徴:タンパク質N末端のグリシン残基にミリスチン酸(C14の飽和脂肪酸)がアミド結合し、**細胞質側(内側)**の膜係留に用いられます。
2. パルミチン酸(Palmitic acid)
- 修飾名:パルミトイル化
- 特徴:タンパク質内のシステイン残基のチオエステル結合にパルミチン酸(C16の飽和脂肪酸)が付加され、疎水性が高まることで細胞質側の膜への強い係留力を発揮します。
3. プレニル基(Prenyl group)
- 修飾名:プレニル化(ファルネシル化やゲラニルゲラニル化)
- 特徴:イソプレン系炭化水素(ファルネシル基C15、ゲラニルゲラニル基C20)がC末端システインに結合し、膜への強固なアンカーとして働きます。これも細胞質側での係留が主です。
細胞外部(反細胞質側)に面した膜タンパク質やグリコシル化プロテオグリカンの係留に使われる脂質
- GPIアンカー(グリコシルホスファチジルイノシトールアンカー)
まとめ表
| 脂質修飾 | 主な用途・側 | 代表例 |
|---|---|---|
| ミリストイル化 | 細胞質側 | Srcファミリーキナーゼなど |
| パルミトイル化 | 細胞質側 | Ras, Gαサブユニットなど |
| プレニル化 | 細胞質側 | Ras, Rab, Ranなど |
| GPIアンカー | 細胞外側(表面側) | アルカリホスファターゼ、プロテオグリカン等 |
→ 細胞外部(反細胞質側)に面したタンパク質やグリコシル化プロテオグリカンの係留には「GPIアンカー」が使われます。
脂質二重層は,二次元の流動層と考えられる。これはどんな意味か.二重層内での脂質分子やタンパク質の動きを駆動するのは何か。こうした動きはどうやって測るのか。膜の流動性に影響を与える因子は何か
「脂質二重層は二次元の流動層と考えられる」とはどういう意味か?
脂質二重層は、細胞膜の基本構造で、多数のリン脂質分子が二層に並び、両端が水に親和性をもつ「親水性頭部」、内側が水を嫌う「疎水性脂肪酸」になっています。
この二重層では、各脂質分子や膜タンパク質が膜の平面(横方向・二次元)内で自由に動き回れる(拡散できる)性質があり、まるで“薄い液体のシート”のようにふるまいます。
ただし、膜の厚み方向(縦方向)に移動するのは非常に難しいです。したがって「二次元の流動層」と表現されます。
二重層内での脂質分子やタンパク質の動きを駆動するのは何か?
**主な駆動力は「熱運動(ブラウン運動)」**です。
細胞温度で分子が常に微細に振動・移動しており、このエネルギーによって脂質やタンパク質がランダムに二次元面内を移動できます。
この拡散運動には、分子サイズ、膜の粘性、周囲の分子密度なども関係します。
こうした動きはどうやって測るのか?
いくつか代表的な生体膜の分子運動の測定法があります。
- FRAP(蛍光退色回復法):脂質やタンパク質を蛍光で標識し、一部をレーザーで退色させた後、蛍光がどれだけ速やかに回復するか(=どれだけ分子が動いているか)を測る方法です。
- シングルモレキュールイメージング(単一分子追跡):個々の分子の動きをリアルタイムで追跡することで拡散速度や動き方を解析します。
膜の流動性に影響を与える因子は何か?
- 温度 : 温度が高いほど分子はよく動く(流動性↑)、低いと動きにくい(流動性↓)。
- 脂肪酸鎖の性質 :
- 鎖が短く不飽和(二重結合が多い)ならパッキングが緩くなり流動性↑。
- 鎖が長く飽和ならパッキングが密になり流動性↓。 - コレステロール : コレステロールが多いと膜の硬さや流動性が調整され、流動性を程よく保つ助けとなる。
- タンパク質や糖鎖の密度 : タンパク質が多いと脂質同士の動きはやや妨げられる。
- 脂質ドメインの形成 : スフィンゴ脂質やコレステロールに富む「ラフト」領域は、通常よりも硬く流動性が下がることがある。
まとめると、脂質二重層という細胞膜は、成分分子が膜の面内で自由に行き来できる「二次元の液体」としてふるまっており、その動きは熱運動によって駆動されます。流動性は脂質の種類・温度・コレステロール量など複数の要因によって調節され、その可動性はFRAPなどの方法で観察・測定できます。
小胞体と細胞質の間でのリン脂質の生合成では、細胞によって解決されなければならない問題がいくつかある。以下のそれぞれはどのように対処されているか説明せよ。a. リン脂質の生合成の基質はすべて水溶性である。しかし、最終産物は水に不溶性である。b. すべての新しく生合成されたリン脂質を取込む箇所は、小胞体膜の細胞質側リーフレットである。しかし、リン脂質は膜の両側に組込まれなくてはならない。c. 細胞の多くの膜系(たとえば細胞膜)は、自身のリン脂質を合成することはできない。しかし、これらの膜は、細胞が成長したり分裂したりするとき、拡張されなければならない。
a. リン脂質の生合成の基質はすべて水溶性である。しかし、最終産物は水に不溶性である。
リン脂質の合成酵素は小胞体膜(ER膜)に埋め込まれています。
基質(グリセロールや脂肪酸、CDP-コリン/エタノールアミンなど)は水溶性で、細胞質側から酵素の作用部位に供給されます。
合成が進むにつれ脂質分子として疎水性が強くなっていくため、生成されたばかりのリン脂質はそのまま膜の疎水性領域へ自発的に埋め込まれ、水相には拡散しません。つまり、1分子ごとに「水溶性→疎水性」にスムーズに移行できるように、合成酵素の配置や触媒経路が調節されています。
b. すべての新しく生合成されたリン脂質を取込む箇所は、小胞体膜の細胞質側リーフレットである。しかし、リン脂質は膜の両側に組込まれなくてはならない。
リン脂質合成は基本的に小胞体膜の細胞質側(外側)リーフレットで起こりますが、膜の安定性や厚み・対称性を保つため脂質分子は膜の両側(外葉・内葉)に均等に存在する必要がある。
この問題に対処するため、
- フリッパーゼ、フロッパーゼ、スクランブラーゼなどの「脂質トランスロケーター酵素」が膜に存在し、リン脂質を一方のリーフレットからもう一方へ“移動(トランスロケーション)”させます。
- これにより新しくできたリン脂質が自然と膜の両側に分配され、膜構造が均一に維持されます。
c. 細胞の多くの膜系(たとえば細胞膜)は、自身のリン脂質を合成することはできない。しかし、これらの膜は,細胞が成長したり分裂したりするとき、拡張されなければならない。
ほとんどのリン脂質の生合成は小胞体でのみ進行し、ゴルジ体や細胞膜自身では新規合成できません。
このため、
- 小胞体で作られたリン脂質は輸送小胞(ベシクル)や脂質搬送タンパク質を介して、他の細胞内膜(ゴルジ体や細胞膜)へ運ばれます。
- 輸送小胞は膜成分とともに各所とくっつくことで、必要な場所へリン脂質を届け、膜が拡張・維持されます。
- こうして細胞分裂や成長に合わせて全ての膜がバランス良く増え続けます。
まとめ:
a→合成酵素の配置と反応経路によって水溶性→疎水性への連続的変換が実現されています。
b→脂質トランスロケーター(フリッパーゼ等)が膜両側に均等にリン脂質を分配します。
c→輸送小胞や搬送タンパク質が小胞体から他の膜へリン脂質を供給します。
脂肪酸が細胞内で移動するためには脂質シャペロンが必要である。なぜそうしたシャペロンが必要なのか。脂肪酸の細胞内輸送にかかわっているタンパク質群は何とよばれているか。脂肪酸の細胞内輸送にかかわるこれらのタンパク質の重要な特徴は何か。
なぜ脂肪酸の移動に脂質シャペロンが必要なのか?
脂肪酸は炭化水素鎖(疎水性部分)が長いため、水(細胞質)にはほとんど溶けません。細胞の中は水で満たされているので、脂肪酸がそのままでは自由に細胞内を移動できず、すぐに集合したり細胞に障害を与える可能性があります。
そのため、脂質シャペロン(脂質結合タンパク質)が脂肪酸分子を包むことで、細胞内の水の多い環境でも安全・効率的に運搬できるようにしています。
脂肪酸の細胞内輸送に関わるタンパク質群の名称
これらのタンパク質群は**脂肪酸結合タンパク質(Fatty Acid Binding Proteins:FABP)**と総称されます。
FABP以外にも、脂肪酸トランスロカーゼやアポリポタンパク質など脂質保存・輸送に関係するタンパク質がありますが、“細胞内”で主に働くのはFABP群です。
FABPなど、脂肪酸の細胞内輸送に関わるタンパク質の重要な特徴
- 小型かつ疎水性ポケットを持っている:
FABPなどは脂肪酸(疎水性分子)を“内側のポケット”に結合させ、外側は親水性に保つことで、水中でも脂肪酸を安定して運搬できます。 - 脂肪酸に対する高い親和性と選択性:
様々な種類の脂肪酸や関連分子ごとに特異的なFABPが存在し、運ぶべき場所・役割ごとに使い分けられています。 - 細胞内局在の違い:
FABPは細胞質だけでなく、核FABPやミトコンドリア型FABPなど、特定の細胞内区画にも分布し、それぞれの役割(エネルギー供給、シグナル伝達、膜構成など)を補助しています。
まとめ:
脂肪酸は水に溶けず細胞内を自由に移動できないため、FABPなどの脂質シャペロンが必要です。これらのタンパク質は疎水性分子である脂肪酸を安全・効率よく運ぶための“結合ポケット”を持ち、脂肪酸ごとに高い選択性・親和性・局在性があることが大きな特徴です。
グリセロリン脂質に共通する脂肪酸鎖は何か。また、なぜこれら脂肪酸鎖の炭素数は 2の倍数になっているのか。
グリセロリン脂質に共通する脂肪酸鎖とは?
グリセロリン脂質は、グリセロール骨格のsn-1およびsn-2位に脂肪酸鎖がエステル結合した構造を持つリン脂質の一群です。共通して持つのは、
- 2本の脂肪酸鎖(アシル鎖)であることです。
- これらの脂肪酸鎖は一般に長鎖脂肪酸で、14〜24個の炭素を持ちます。
- 脂肪酸は通常、飽和または不飽和(二重結合を持つ)で生体膜の流動性や特性を決定づけます。
炭素数がなぜ2の倍数なのか?
脂肪酸鎖の炭素数が2の倍数である理由は、生体内の脂肪酸合成の過程に由来します。
- 脂肪酸は主にアセチルCoA(2炭素単位)から繰り返し2炭素ずつ付加されて伸長されます。
- この合成反応は脂肪酸合成酵素複合体によって制御され、1回の反応で2炭素単位(マロニルCoA由来)が連結されるため、最終的にできる脂肪酸の炭素数は必ず2の倍数になります。
- これが生体内の脂質構成の基本的な特徴です。
まとめ
- グリセロリン脂質はグリセロール骨格に2本の脂肪酸鎖を結合し、これらは主に長鎖脂肪酸で構成されている。
- 脂肪酸合成過程が2炭素単位の付加を繰り返すため、脂肪酸鎖の炭素数は一般に2の倍数になる。
この基本的な構造パターンが生体膜の安定性や物理化学的性質を支えています。
コレステロールの生合成は、高度に調節された過程である。
コレステロール生合成において、重要な調節を受ける酵素は何か。この酵素はフィードバック阻害を受ける。フィードバック阻害とは何か。この酵素は細胞内のコレステロール量をどのように感知するのか。
コレステロール生合成で重要な調節を受ける酵素
コレステロールの生合成経路で**最も重要な調節ポイントとなる酵素は、「HMG-CoA還元酵素(HMG-CoA reductase)」**です。
この酵素は、メバロン酸への変換を触媒し、生合成経路の律速段階に位置しています。
フィードバック阻害とは何か
フィードバック阻害とは、生合成経路の最終産物(ここではコレステロール)が、その経路内の初期の段階で活性を調節し、自らの過剰合成を防ぐ制御機構です。
つまり、コレステロール量が十分または過剰だと、HMG-CoA還元酵素の活性や発現が抑制され、コレステロールの過産生が防がれます。
HMG-CoA還元酵素は細胞内のコレステロール量をどのように感知するのか
細胞はコレステロール量を直接「感知」しているわけではなく、コレステロール量の変化に応じた複雑なタンパク質制御系を通じて調節が行われます。
- コレステロール量が増えると、小胞体膜に存在する膜タンパク質「SCAP(SREBP cleavage-activating protein)」とコレステロール受容体「Insig」が複合体を形成。
- この複合体は転写因子SREBP(Sterol Regulatory Element-Binding Protein)のクロア膜から核への移行を阻害し、HMG-CoA還元酵素遺伝子の転写を抑制します。
- またコレステロールの増加は、HMG-CoA還元酵素の速やかな分解(小胞体関連分解:ERAD)も促進し、酵素量を減らします。
以上の制御を通して、細胞内のコレステロール量に応じてHMG-CoA還元酵素の活性・量がフィードバック制御され、コレステロール生合成が巧みに調節されています。
まとめ
- 重要な調節酵素は「HMG-CoA還元酵素」。
- フィードバック阻害は「最終産物が初期酵素を抑える自己調節機構」。
- 細胞内コレステロール量は、SCAP-Insig複合体とSREBP転写因子の動き、さらに酵素の分解速度を通じて間接的に感知・制御されている。
この仕組みによりコレステロールの恒常性が保たれているのです。
コレステロールは哺乳類の細胞膜内において最も普遍的な脂質分子なので,その機能のひとつは構造の維持であることは明白である。しかし、コレステロールはほかにも機能をもっている。コレステロールは多機能的な膜脂質であるという結論に導くコレステロールとその代謝の特徴は何か。
コレステロールの多機能性を示す特徴と代謝のポイント
- 膜構造の調節機能
- コレステロールは細胞膜の流動性や剛性を調節し、脂質二重層の物理的・化学的安定性を高めます。
- 膜の厚みや透過性も調節し、細胞の環境変化に対して膜を安定に保ちます。
- さらに、スフィンゴ脂質と共に「脂質ラフト」と呼ばれる特殊な膜ドメインを形成し、ここでのシグナル伝達や膜タンパク質の集積に関与します。
- シグナル分子・前駆体としての役割
- コレステロールは、ステロイドホルモン(性ホルモン・糖質コルチコイドなど)やビタミンDの前駆体となる重要分子であり、幅広い生理機能に関わります。
- また、胆汁酸の合成原料でもあり、脂質の消化と吸収にも必須です。
- 代謝の高度な調節
- コレステロールの合成、取り込み(LDL受容体経路)、排出、エステル化は極めて精密に制御されており、細胞内と血中のコレステロール量の厳密な恒常性維持に貢献しています。
- 代謝異常は動脈硬化やライソゾーム病など多様な疾患につながる。
- 膜の動的調節に関わる役割
- コレステロールは、膜タンパク質の活性やシグナル伝達経路の調節、細胞間情報伝達に重要な役割を果たしています。
- たとえば受容体のクラスター形成やエンドサイトーシスの効率化などに関与します。
まとめ
- 細胞膜の物理化学的安定性の維持に大きく寄与する一方、
- ステロイド合成やビタミンDの前駆体など多彩な生理機能をもち、
- 分解産物の調節や膜シグナル伝達においても重要な役割を果たすため、コレステロールは多機能的な膜脂質といえる。
この幅広い機能性と高度な代謝制御機構が、コレステロールの生体膜脂質としての地位を決定づけているのです。
リン脂質とコレステロールは、細胞内の合成部位からさまざまな膜系へと輸送されなければならない。この方法のひとつは小胞輸送であり、多くのタンパク質を分泌する経路もこれによって行われる。しかし、ほとんどのリン脂質およびコレステロールの膜間輸送は、ゴルジ体を介した小胞輸送によるものではない。この記述の根拠は何か。また、リン脂質とコレステロール輸送のおもだった機構はどんなものか。
1.この記述の根拠
- タンパク質の分泌経路では、小胞体からゴルジ体を通り、輸送小胞を介して細胞膜へ運ばれますが、脂質の多くの種類はこの経路を主に通っていません。
- 脂質、特にリン脂質とコレステロールはゴルジ体を含む小胞輸送系に乗る量が非常に少ないことが、実験的に示されています。
- 小胞は膜の一部を切り取って輸送するため、膜の成分は多少しか含めません。一方、多量の脂質輸送は小胞に依存すると膜の組成が著しく変わってしまうリスクがあります。
- 膜の脂質組成の均一性や恒常性を保つためには、小胞輸送だけでは不十分であり、異なる輸送経路があることが根拠です。
2.リン脂質とコレステロール輸送のおもだった機構
- 膜接合(メンブレインコンタクトサイト、MCS)を介した非小胞輸送
- 小胞体と他の細胞内膜(ミトコンドリア、ゴルジ体、細胞膜など)が直接接触し、脂質搬送タンパク質(LTP:lipid transfer proteins)が脂質を媒介的に運ぶ。
- これにより、脂質は小胞を介さずダイレクトに膜間で交換・補充されます。
- 例:ORPファミリーやスタル酸結合タンパク質などがLTPとして機能。
- 輸送小胞を介する従来の経路
- ゴルジ体を通る分泌経路で、一部の脂質も含まれるが、主要経路ではない。
- 脂質シャペロンタンパク質による細胞質内輸送
- 脂肪酸や一部の疎水性脂質は脂質結合タンパク質(FABPなど)により細胞質内輸送される。
- 膜融合による直接輸送
- 膜同士が融合して脂質成分が直接移動する場合もある。
まとめ
- 多くのリン脂質とコレステロールは、小胞輸送系(特にゴルジ体を経由する経路)だけではなく、膜接合サイトを介した非小胞性の直接輸送が主な輸送経路である。
- これは、小胞輸送だけでは膜脂質の均一な組成維持や量的補充が難しいため、専用の脂質搬送タンパク質によるダイレクトな膜間輸送機構が発展した結果とされる。
このような多様な機構が細胞膜やオルガネラ膜の脂質組成の恒常性を確保しています。
次の文章を説明せよ。すべての生体膜の構造は、リン脂質の化学的な性質に依存している。一方、特定の生体膜の機能は、この膜に結合した特定のタンパク質に依存している。
すべての生体膜の構造は、リン脂質の化学的な性質に依存しているとは?
生体膜は主にリン脂質(リン酸+脂肪酸鎖)からできています。リン脂質は「両親媒性分子」で、
- 親水性の「頭部」(リン酸基など)が水になじみやすく、
- 疎水性の「尾部」(脂肪酸鎖)が水を避ける性質を持っています。
このため、リン脂質分子は水がある環境下で自発的に脂肪酸尾部同士が内側に集まり、親水性頭部は外側に向かう脂質二重層を形成します。
これが細胞膜の「基本構造」であり、細胞膜が薄い膜のように細胞内外を仕切る物理的基盤となっています。
つまり、生体膜の物理的・化学的な安定性はリン脂質の「親水性・疎水性の両親媒性」という化学的性質に大きく依存しているのです。
特定の生体膜の機能は、この膜に結合した特定のタンパク質に依存しているとは?
生体膜には脂質だけでなく、多種多様な膜タンパク質が埋め込まれたり、付着したりしています。
これら膜タンパク質は、膜の物理的構造とは別に、以下のような特別な機能を担っています。
- 物質の輸送:イオンチャネルやトランスポーターによる物質の出入りの制御。
- シグナル伝達:受容体タンパク質が外部からの信号を受け取り、細胞内に情報を伝える。
- 細胞接着:膜タンパク質同士の結合により細胞同士や細胞外マトリックスと結合。
- 酵素活性:膜上での化学反応促進。
- 細胞骨格との連結:膜の形状や動きを制御。
つまり、生体膜の機能は、リン脂質の物理的な二重層内に埋め込まれた「特定の膜タンパク質」によって実現されているのです。
まとめ
- 生体膜の「構造」はリン脂質の両親媒性化学性質による脂質二重層形成に依存する。
- 生体膜の「機能」は、それに結合する膜タンパク質の種類や配置、作用に依存する。
- この両者の組み合わせにより、細胞膜は物理的なバリアとしてだけでなく、生体の情報伝達や物質輸送など多様な役割を果たせる。
これが現代の細胞膜モデル(流動モザイクモデル)の基本的な理解です。
膜に結合しているタンパク質を三つに分類したとき、それぞれをどんな名称でよぶか、それぞれの分類に属するタンパク質が生体膜と結合する機構を解説せよ。
膜に結合しているタンパク質は、一般に以下の3つの分類に分けられます。
1. 内在性膜タンパク質(Integral membrane proteins)
- 特徴:タンパク質の一部または全体が脂質二重層の中に埋め込まれている。
- 結合機構:
- 膜の疎水性部分(脂質の脂肪酸鎖)に、タンパク質の疎水性アミノ酸配列(主にαヘリックスやβバレル構造)が直接結合。
- 膜を一回または複数回貫通することが多い。
- 脂質と強固な疎水性相互作用で結びつき、その除去には界面活性剤等の強い化学処理が必要。
- 例:イオンチャネル、輸送体、受容体など。
2. 表在性膜タンパク質(Peripheral membrane proteins)
- 特徴:膜の表面に弱く結合し、脂質二重層の内外両面に存在する。
- 結合機構:
- 脂質の親水性頭部や内在性膜タンパク質の外側ドメインと静電相互作用や水素結合、一時的な結合で結びつく。
- 高塩濃度やpH変化で容易に遊離する。
- 例:細胞骨格関連タンパク質、シグナル伝達分子など。
3. 脂質アンカー型膜タンパク質(Lipid-anchored proteins)
- 特徴:タンパク質自体は疎水性膜貫通領域を持たず、脂質修飾により膜に係留されるタイプ。
- 結合機構:
- タンパク質に共有結合的に脂肪酸鎖(例:ミリストイル、パルミトイル)やプレニル基、GPIアンカー(グリコシルホスファチジルイノシトール)が付加され、脂質二重層の疎水性部分に埋め込まれる。
- タンパク質本体は膜から離れているが、脂質鎖により固定される。
- 例:GPIアンカー型タンパク質、細胞質側にミリストイルやパルミトイル修飾のあるタンパク質。
まとめ表
| タンパク質の種類 | 膜との結合の特徴 | 結合の仕組み | 代表的な例 |
|---|---|---|---|
| 内在性膜タンパク質 | 脂質二重層を貫通し強固に結合 | 疎水性の膜貫通ドメインによる直接的疎水結合 | イオンチャネル、輸送体、受容体 |
| 表在性膜タンパク質 | 膜表面に一時的・弱く結合 | 静電的相互作用、タンパク–タンパク相互作用 | 細胞骨格結合タンパク質など |
| 脂質アンカー型膜タンパク質 | タンパク質自体は膜非貫通、脂質修飾で膜にアンカー | ミリストイル、パルミトイル、GPIアンカーなどの脂質修飾 | GPIアンカータンパク質、脂肪酸修飾タンパク質 |
これら三種類の膜タンパク質の結合機構の違いにより、生体膜は多様な機能を実現しています。
生体膜の両面は主として脂質やタンパク質といった同じような成分でできているが、両者の組成は同一ではない。何が両面の非対称性を生み出すか。
生体膜の非対称性とは
生体膜はリン脂質やタンパク質などの成分からできていますが、膜の「外側(細胞外側)」と「内側(細胞質側)」では、その組成が異なります。このことを「膜の非対称性」と言います。
なぜ非対称性が生まれるのか
- 脂質合成と膜への挿入の過程
- 多くのリン脂質は小胞体(ER)で合成され、主に膜の細胞質側リーフレット(半膜)に最初に挿入されます。
- 脂質は膜の内外を自発的に自由に行き来できず、特殊な酵素(フリッパーゼ・フロッパーゼ・スクランブラーゼ)によって特定の脂質が一方の側に移されることで非対称性が形成・維持されます。
- タンパク質の局在・付加の偏り
- 糖脂質やスフィンゴ脂質は主に細胞の外側に多く存在し、そこに結合したタンパク質は外側に局在します。
- 一方、リン脂質の種類(例:ホスファチジルセリンやホスファチジルエタノールアミン)は細胞質側に偏在し、膜の内外で機能が異なります。
- 細胞の能動的エネルギー消費による維持
- 脂質の移動はランダム拡散だけでは起こらず、多くの場合ATPなどのエネルギーを使って非対称性が積極的に維持されます。
非対称性がもたらす生理的意義
- 細胞機能の分化:膜の内外で異なるシグナル伝達や物質輸送が実現される。
- 細胞認識や接着:糖脂質を含む膜外側は細胞外環境との相互作用に重要。
- アポトーシスのシグナル:例えばホスファチジルセリンが内側から外側に露出することで細胞死シグナルになる。
まとめ
膜の非対称性は、脂質合成過程における膜への挿入面の不均一性、脂質を特異的に移動するタンパク質、そしてタンパク質や糖鎖の偏りによって生まれ、エネルギー依存的に維持される生体膜の基本的特徴です。この非対称性は、細胞の多様な生命活動に欠かせない重要な構造的基盤となっています。
問題文引用元:東京化学同人 分子細胞生物学 第6版

コメント